La recherche clinique est une des missions de l’ICM. Les essais cliniques permettent d’utiliser aujourd’hui les médicaments ou les stratégies thérapeutiques de demain.
Objectifs de la recherche clinique
La recherche clinique vise à faire progresser et améliorer, dans le respect de l’éthique, les prises en charge thérapeutiques, les techniques de soins, de diagnostic ou de prévention à travers l'élaboration et la réalisation de projets de recherche innovants.
Les essais cliniques permettent d'évaluer :
- un nouveau médicament (ou une nouvelle association thérapeutique),
- une nouvelle façon de les administrer (par comprimés plutôt que par injection par exemple)
- des techniques novatrices de traitement (radiothérapie ou chirurgie) ou de diagnostic (test biologique par exemple).
Leur finalité est de déterminer si ces nouveaux traitements sont efficaces, bien tolérés et susceptibles d'être, à terme, proposés à tous les patients concernés.
Les essais cliniques sont des étapes indispensables dans la mise à disposition d'un nouveau traitement : c’est l’évaluation et la validation chez l’homme des traitements identifiés comme prometteurs suite aux études précliniques effectuées en laboratoire.
Déroulement d'un essai clinique
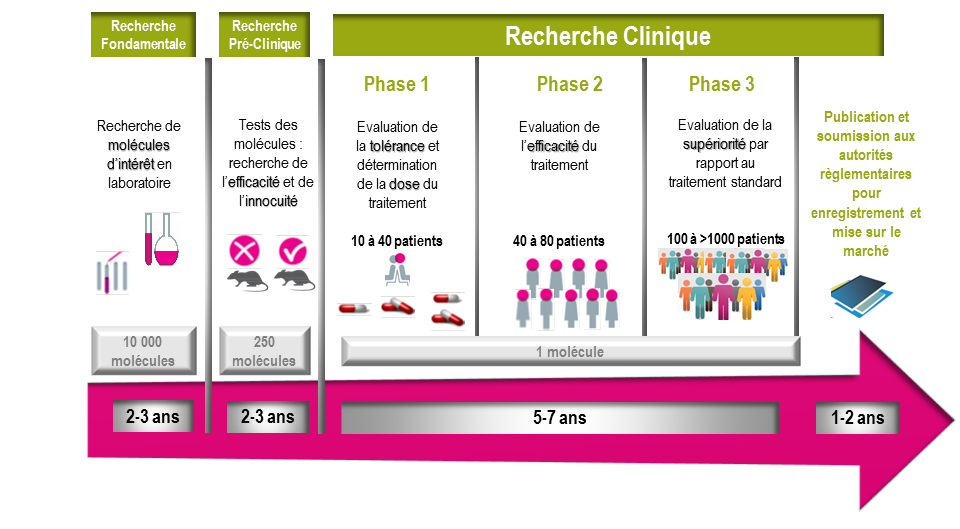 Il faut généralement plus de 10 ans pour qu’une molécule puisse être prescrite à un patient. Les essais cliniques permettent:
Il faut généralement plus de 10 ans pour qu’une molécule puisse être prescrite à un patient. Les essais cliniques permettent:
- De déterminer la dose et d'évaluer la tolérance du produit,
- D’évaluer son efficacité,
- Enfin de démontrer une efficacité supérieure de ce nouveau traitement par rapport au traitement de référence.
Qu'est-ce qu'un essai clinique en oncologie ?
Réglementation en recherche clinique
Les essais cliniques sont soumis à une règlementation spécifique et sont menés selon des protocoles scientifiques rigoureux. Ils sont réglementés par les lois relatives à la politique de santé publique et aux recherches biomédicales. Les Comités de Protection des Personnes (CPP) et l’Agence Nationale de Sécurité du Médicament et des produits de santé (ANSM) sont chargés de contrôler la pertinence du projet (intérêt scientifique et médical) et la protection des personnes qui vont y participer.
La participation à un essai clinique est libre et volontaire (Loi Huriet- Sérusclat n°88-1138 du 20/12/1988).
Après accord des autorités de santé, les essais cliniques sélectionnés par les médecins de l’ICM sont validés à l’ICM par la COmmission interne de MEthodologie en REcherche clinique (COMERE) avant d’être mis en place. Les projets de recherche translationnelle, de création de collections et de cession de ressources biologiques sont, eux, soumis à l’avis du Comité de Recherche Translationnelle (CORT).

Recherche clinique intégrée à votre parcours de soins à l’ICM
Les essais cliniques font partie de l'activité médicale quotidienne de l’ICM. Ils s’adressent à toutes les disciplines liées à la thérapeutique du cancer (chirurgie, radiothérapie, oncologie médicale, imagerie...) ainsi qu’aux soins dispensés pendant ou après les traitements oncologiques (psycho-oncologie, activité physique, kinésithérapie, hypnose … appelés soins de support). Ils sont proposés par les médecins à leurs patients dès que cela est possible. Le parcours de soins est alors coordonné par un Attaché de Recherche Clinique (ARC), tout en restant intégré à la prise en charge globale de l’ICM.
Participation à un essai clinique
La participation à des études cliniques peut vous être proposée au cours de votre prise en charge à l’ICM. Elle permet souvent d’accéder à des innovations thérapeutiques. Si vous deviez décider de ne plus participer à un essai, vous pourrez le quitter de votre gré à tout moment et bénéficierez d'un autre traitement adapté à votre maladie. Cette décision ne remettra pas en cause l'engagement de l'équipe médicale à vous soigner.
Retrouvez quelques définitions sur ce lien

Accepter de participer à un essai clinique, c’est comme se lancer un défi. Je me sens entouré, il y a toujours quelqu’un pour répondre à mes questions. C’est rassurant.
La recherche clinique expliquée en vidéo
Organisation de la recherche clinique à l’ICM
L’activité de promotion de la recherche clinique à l’ICM est assurée par la DRCI (Direction de la Recherche Clinique et de l’Innovation).
Les activités d’investigation de la recherche clinique sont assurées par le CRC (Centre de Recherche Clinique) et par le CIPP (Centre d'Investigation de Phase Précoce).
En tant que CLCC, l’Institut associe recherche fondamentale, translationnelle et clinique pour développer une recherche intégrée sur le cancer, centrée sur le patient.
Ainsi, les unités de la recherche clinique travaillent en étroite collaboration avec les équipes de biométrie, du CEPP, du CRB, de l’URT, de l’Innovation technologique et sont regroupés au sein d’une direction unique : la Direction Scientifique.
Dans le cadre de Montpellier Cancer, l’ICM fait partie des 8 centres en France labellisés Site de Recherche Intégrée en Cancérologie (SIRIC) par l’Institut National du Cancer (INCa).

"De la Recherche au Patient"
L'ICM vous propose de découvrir la réalité des équipes de recherche clinique au travers de photographies montrant leur quotidien et leur contribution à l'innovation thérapeutique en cancérologie au service de nos patients.
Ce reportage a été réalisé par Sophie Pattingre, chercheuse à l'IRCM et passionnée de photographie.
us propose de découvrir la réalité des équipes de recherche clinique au travers de cette exposition de photographies.

Certification ISO 9001
Les unités de Recherche Clinique et Biométrie de l’ICM ont été officiellement certifiées ISO 9001 par l’AFNOR Certification depuis août 2017.
La certification ISO 9001 est une norme internationale qui définit des exigences pour la mise en place d'un Système de Management de la Qualité (SMQ). Celle-ci est attribuée pour une durée de 3 ans. Elle a été renouvelée en 2020 pour 3 ans supplémentaires.
Internationalement reconnue, la norme ISO 9001 permet de garantir à tous, patients, médecins et partenaires, un haut niveau de qualité et de sécurité dans la gestion des projets.
L'ICM certifié
L'ICM est, aujourd'hui, le seul établissement de la région Occitanie Méditerranée, à obtenir cette certification qui a mobilisé plus de 90 personnes pendant plus d'une année.
Une politique qualité été élaborée en cohérence avec les orientations stratégiques déclinées dans chacun des secteurs de la recherche clinique et de la biométrie, selon 4 axes. Elle témoigne de la volonté de la Direction et des responsables des Unités de mettre en œuvre une démarche d'amélioration continue, avec pour enjeux :
- Répondre aux attentes des clients et des parties intéressées
- Améliorer en continu l'organisation des unités
- Permettre à la Direction Générale d'avoir une visibilité sur la démarche des unités.


